Definicion De Combustion Completa
La combustión se considera que es una de las primeras reacciones químicas controladas intencionalmente por los seres. Tristes son las pérdidas debidas a una única molécula química.
Combustion Concepto Reaccion Etapas Tipos Y Ejemplos
La combustin es generalmente entendida como sinnimo de arder pero desde un punto de vista qumico la combustin es un fenmeno mucho ms amplio.

Definicion de combustion completa. La combustión es una reacción química exotérmica entre dos reactivos combustible y comburente en los que se produce liberación de energía en forma de calor. En realidad se trata de una combustión ideal que solo puede conseguirse en laboratorio. Desde el punto de vista científico la combustión se describe como un proceso de.
En este tipo de reacción no se encontraran sustancias combustibles en los humos o gases de combustión. 6730 - Combustión Unidad I. Los tipos más frecuentes de combustible son las materias orgánicas que contienen carbono e hidrógeno ver hidrocarburos.
Toda combustión completa libera como producto de la reacción dióxido de carbono CO2 y agua en estado de vapor H2O. Definición de reacción de combustión La reacción de combustión se basa en la reacción química exotérmica de una sustancia o una mezcla de ellas denominada combustible con el oxígeno. Caracteristicas Procesos de combustidn Tal vez el proceso tCrmico de mayor inter prictico por su escala de utilizaci6n mundial siendo a la vez muy ficil de realizar y muy dificil de estudiar sea el proceso de reacci6n quimica exot6rmica automantenida por conducci6n de calor y difusi6n de especies conocido.
Índice Ocultar 1 Características. Combustión completa Cuando al reaccionar una sustancia orgánica con el oxígeno el producto resultante es sólo CO 2 g y H 2 O l. Combustión completa y combustión incompleta.
Esto es la combustión completa se produce cuando el total del combustible reacciona con el oxígeno es decir cuando toda la parte combustible se ha oxidado al máximo es decir no quedan residuos de combustible sin quemar. Según la cantidad de oxígeno disponible la combustión también se clasifica en completa e incompleta. Las moléculas encierran energía en sus.
Cabe mencionar que esta combustión es igual a la combustión completa ya que también se produce agua. La combustión es una reacción química que se produce entre un combustible y un agente oxidante que produce energía generalmente en forma de calor y luz. Combustión Te explicamos qué es la combustión cómo se produce y cuáles son las etapas de la reacción.
En este tipo de combustión los productos conocidos como pirólisis permanecen sin quemar por lo que contaminan el humo resultante mediante la producción de gases nocivos. La ola de frio en la que estamos sumergidos nos trae malas noticias año tras año. La combustión es la reacción de oxidación completa de moléculas orgánicas produciendo CO2 y agua.
La Combustión Estequiométrica o neutra es otro tipo de combustión. En una reacción completa todos los elementos que forman el. La combustión completa es una reacción química en la que todos los átomos de carbono de una sustancia en particular se consumen por completo.
La forma general de una reacción de combustión puede ser representada por la reacción entre un hidrocarburo y oxígeno que produce dióxido de carbono y agua. La palabra proviene del latín combustio y combustioni con el mismo significado. Este es el nombre dado a las combustiones completas las cuales ocurren cuando el metano se transforma en CO2 y H2O usan las cantidades correctas de oxígeno para su reacción y que generalmente ocurren solo en el ambiente controlado de un laboratorio haciendo uso de instrumentos requeridos por ejemplo en el caso del metano en polvo se utiliza la cucharilla de combustión.
Viendo el ejemplo anterior de la combustión del metano se puede ver que se necesitan dos moléculas de O 2 para la combustión de una molécula de CH 4. La combustión se considera un exergónica o exotérmica reacción química. COMBUSTIN COMPLETA E INCOMPLETA.
Reacción de Combustión En este contexto la reacción de combustión nombre usual de las reacciones de oxidación de compuestos químicos con el oxígeno del aire es el principal agente de los procesos térmicos donde tanto la cinética cuanto el grado de mezcla del combustible y oxidante influencian en el comportamiento de la llama. También es conocida como la quema. Cuando las reacciones indicadas están desplazadas totalmente a la derecha es decir los componentes se oxidan completamente formando dióxido de carbono CO 2 agua líquida H 2 O y en su caso dióxido de azufre SO 2 independientemente de la cantidad de aire empleada en la reacciónEsto implica que el oxígeno presente en el aire ha sido cuando menos.
Combustión significa acción y efecto de quemar o arder por completo una determinada materia. Combustión completa o perfecta. Cuando las reacciones indicadas están desplazadas totalmente a la derecha es decir los componentes se oxidan completamente formando dióxido de carbono CO 2 agua líquida H 2 O y en su caso dióxido de azufre SO 2 independientemente de la cantidad de aire empleada en la reacción.
Una reacción de combustión es un tipo de reacción química en la que un compuesto y un oxidante reaccionan para producir calor y un nuevo producto. La combustión completa es casi imposible de lograr. Sin embargo en lugar de dióxido de carbono el producto es carbono y monóxido de carbono.
Combustión completa Como se menciono anteriormente en la combustión completase queman las sustancias combustibles del combustible hasta el máximo grado posible de oxidación. Si hay suficiente oxígeno habrá una combustión completa en. Esta es una combustión completa en la que se ha empleado la cantidad exacta de aire obtenida a partir de las relaciones cuantitativas de las moléculas que intervienen en cada reacción.
La combustin se puede definir como una reaccin de oxidacin altamente exotrmica lo que significa que es una reaccin que desprende energa en forma de calor a veces acompaada de luz como ocurre en el. Hidrocarburo o 2 co 2 h. Los incendios ciertamente son.
No importa cuál sea el combustible a quemar. Por lo general se entiende que combustión es sinónimo de quemar aunque la definición química suele ser mucho más amplia que simplemente arder con llamas o fuego. En realidad a medida que las reacciones de combustión reales lleguen al equilibrio constante estarán presentes una gran variedad de especies mayores y menores como el monóxido de carbono y el carbono puro hollín o ceniza.
Además clasificación y ejemplos. 4 Entalpía de combustión. Caso estas sustancias también pasarán en forma completa a los humos.

Combustion Que Es Definicion Historia Tipos De Combustion

20 Ejemplos De Reacciones De Combustion

Combustion Definicion Significado

Introduccion A Los Procesos De Combustion Youtube

Que Diferencia Combustion Completa E Incompleta Curiosoando

Reaccion De Combustion Combustion Definicion Ejemplos Experiments Incompleta Reaccion Science Sp Tipos Glogster Edu Interactive Multimedia Posters

Tipos De Combustion Sus Fases Y Algunos Ejemplos
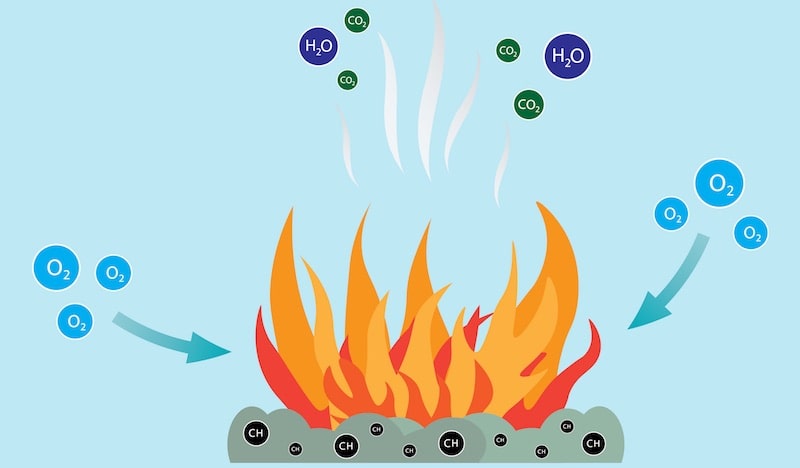
Combustion Concepto Reaccion Etapas Tipos Y Ejemplos

Que Diferencia Combustion Completa E Incompleta Curiosoando

Que Diferencia Combustion Completa E Incompleta Curiosoando

Combustion Definicion Y Ecuacion

Combustion Definicion Significado

Que Es La Reaccion De Combustion Naturgy

Reaccion De Combustion Combustion Definicion Ejemplos Experiments Incompleta Reaccion Science Sp Tipos Glogster Edu Interactive Multimedia Posters

Combustion Que Es Definicion Historia Tipos De Combustion



Posting Komentar untuk "Definicion De Combustion Completa"